Metabolic therapies inhibit tumor growth in vivo and in silico
Scientific Reports volume 9, Article number: 3153 (2019)
In vivo (в переводе с латинского «внутри живого») относится к экспериментам с использованием всего живого организма, а не частичного или мертвого организма.In silico — это выражение, используемое для обозначения «выполнено на компьютере или с помощью компьютерного моделирования». Г.Л.
В последние годы исследования рака были успешными благодаря более чувствительным методам обнаружения, целевым системам доставки лекарств и идентификации большого набора генов с разной экспрессией. Однако, хотя большинство методов лечения все еще основаны на антимитотических средствах, которые вызывают широкие вторичные эффекты, возрастает интерес к метаболическим методам лечения, которые могут минимизировать побочные эффекты. В начале 20-го века Отто Варбург обнаружил, что раковые клетки используют цитоплазматическую ферментацию глюкозы в молочную кислоту для синтеза энергии (так называемый «эффект Варбурга»). Наши исследования направлены на то, чтобы изменить этот эффект при перепрограммировании метаболизма раковых клеток. В этой работе мы представляем метаболическую терапию, специально нацеленную на активность специфических ферментов центрального углеродного обмена, сочетая комбинацию биотерапевтических препаратов METABLOC (альфа-липоевая кислота и гидроксицитрат) с Метформином и Диклофенаком, для лечения опухолей, имплантированных мышам. Кроме того, динамическая метаболическая модель, описывающая центральный (базовый) углеродный метаболизм, а также скорость прохождения химических реакций при метаболизме, на которые нацелены лекарственные препараты, позволила имитировать прогрессирование опухолей как у мышей, получавших лечение, так и без лечения, а также выдвигать гипотезы о влиянии лекарств на метаболизм опухолевых клеток. Наша модель предсказывает обратный эффект Варбурга, вызванный метаболической терапией, на опухолевые клетки.
Вступление
Рак — это генетическое заболевание или нарушение обмена веществ? Эта проблема была предметом дискуссий на протяжении истории рака 1,2. Геномная гипотеза рака первоначально возникла с открытием протоонкогенной тирозин-протеинкиназы (Src), ответственной за рак у цыплят. J.Michael Bishop и Harold E. Varmus, два лауреата Нобелевской премии (1989), обнаружили в 1979 году, что мутации в гене src у нормальных цыплят могут привести к раку3. Затем область геномного рака достигла своего пика благодаря полному секвенированию генома человека Международным консорциумом по секвенированию генома человека в 20014. году. Это открыло новые рынки для фармацевтической промышленности, одновременно определяя новые подходы в терапии рака. Например, синтетические препараты, такие как Цисплатин (Cisplatin) и 5-Фторурацил (5-Fluorouracil), были введены в арсенал лекарственных средств, и сейчас являются частью стандартного химиотерапевтического протокола. Однако ограниченный успех этих химиотерапевтических агентов привел к поиску возможностей для новых стратегий. Новая волна идей возникла с разрушительным мега-обзором, направленным на переопределение «отличительных признаков рака» и общих правил, которые регулируют перепрограммирование нормальных клеток в злокачественные опухоли5. Hanahan и Weinberg описали общий молекулярный механизм, участвующий в регуляции пролиферации, дифференцировки и гибели клеток. Действительно, дисфункции на внутреннем «механизме» или в его среде приводят к одному и тому же патогенному фенотипу: «поддержание пролиферативной передачи сигналов, уклонение от подавителей роста, сопротивление гибели клеток, репликативное бессмертие, устойчивый ангиогенез и активация инвазии и метастазирования». Совсем недавно те же авторы предложили обновленную версию предыдущего обзора, в которой были добавлены «два новых признака», в том числе «перепрограммирование энергетического метаболизма и уклонение от разрушения иммунитетом». Эти новые концепции были предметом многочисленных исследований в последние годы7, в том числе в нашей исследовательской группе 8,9,10,11.
На вопрос о том, является ли рак генетическим заболеванием или метаболическим изменением, гипотеза позволила объяснить, как метаболическое перепрограммирование раковых клеток дает им преимущество по сравнению с нормальными клетками 12,13,14. Наши исследования, среди прочего, способствовали реабилитации прошлых исследований немецкого лауреата Нобелевской премии Отто Варбурга, который представил идею метаболических изменений в раковых клетках15. В своей оригинальной статье Варбург (1956) представил концепции «разобщения дыхания» (“uncoupling of respiration”) и «аэробного гликолиза», происходящих в раковых клетках, чтобы объяснить, что раковые клетки полагаются на цитоплазматическую ферментацию глюкозы в молочную кислоту для синтеза энергии (АТФ). чем окислительное фосфорилирование16. Отто Варбург объяснил это наблюдение фенотипическим выражением болезнетворных митохондрий. Эта характеристика раковых клеток, обозначенная как эффект Варбурга, была предметом обширных исследований в последние годы17. Эффект Варбурга дает метаболические преимущества раковой ткани по сравнению с нормальными соматическими клетками. Это было описано как следствие гибридного аспекта метаболизма раковых клеток, когда анаболизм и катаболизм происходят одновременно14. Углеродные субстраты представляют собой катаболизируемые и промежуточные соединения, используемые в качестве основного источника для синтеза строительных блоков (липиды, белки и нуклеиновые кислоты), которые необходимы для роста клеток8,19,20. Этот гибридный метаболизм объясняет, почему нацеливания на один путь с химиотерапевтическим агентом недостаточно, чтобы остановить рост опухоли. Действительно, метаболическое и эпигенетическое перепрограммирование раковых клеток придает метаболическую пластичность их базовому (центральному) углеродному метаболизму (БУМ) (английская аббревиатура (central carbon metabolism ССМ), что может объяснить их приобретенную устойчивость к современным химиотерапиям.
С этой целью интересным подходом будет нацеливание на базовый углеродный метаболизм с использованием метаболических препаратов, которые, как известно, ингибируют специфические ферменты. Среди ферментов базового углеродного метаболизма (БУM) пируватдегидрогеназа (PDH) и АТФ-цитратлиаза (ACL) играют ключевую роль в метаболическом перепрограммировании раковых клеток18. Ферментативный комплекс пируватдегидрогеназа( PDH) превращает пируват в ацетил-КоА и поддерживает цикл трикарбоновых кислот в нормальных клетках. В раковых клетках было показано, что пируватдегидрогеназа(PDH) ингибируется, тогда как АТФ-цитратлиаза(ACL) сверхэкспрессируется. АТФ-цитрат-лиаза превращает цитоплазматический цитрат в оксалоацетат и ацетил-КоА, предшественник синтеза липидов. Другими ключевыми ферментами, играющими основную роль в метаболизме рака, являются лактатдегидрогеназа (ЛДГ) и ферменты, участвующие в реакциях цепи переноса электронов (ETC). Действительно, метаболическая терапия, направленная на эти ферментативные реакции, участвующие в ферментации углеродных ресурсов, может ограничить их поглощение опухолью, чтобы исчез фенотип Варбурга.
Мы использовали альфа-липоевую кислоту (ALA) и гидроксицитрат (HCA), два старых препарата из фармакопеи, нацеленные на пируватдегидрогеназу(PDH) и АТФ-цитратлиазу(ACL), соответственно. Интересно, что нам удалось показать, что комбинация ALA и гидроксицитрата(HCA) глубоко ингибирует культуры трех раковых клеточных линий (рак мочевого пузыря MBT-2, меланома B16-F10 и рак легких LL/2)21. Эти результаты согласуются с результатами, полученными от Hatzivassiliou и его коллег, которые сообщили об ингибировании роста раковых клеток при использовании специфической молчаливой РНК (SiRNA) для уничтожения экспрессии белка АТФ-цитратлиаза(ACL)22. Аналогичным образом, исследование, проведенное Bonnet и коллегами (2006), продемонстрировало эффективность небольшой молекулы дихлорацетата в восстановлении активности пируватдегидрогеназы (PDH) в раковых клетках23. Взятые вместе, эти экспериментальные результаты показывают потенциал нацеливания на ферменты, участвующие в программировании эффекта Варбурга. Эти терапевтические подходы показывают такую же эффективность, что и обычные методы лечения, но без каких-либо побочных эффектов. Кроме того, мы также исследовали эффективность нашей комбинации лекарств, а именно METABLOC (ALA и HCA), используемой синергитически со стандартными химиотерапевтическими препаратами, такими как Цисплатин или Метотрексан24. Мы сообщили об увеличенной задержке роста опухоли, когда Цисплатин и Метотрексан применяются в комбинации с METABLOC. Стандартизированный метод скрининга позволяет определить лучшие комбинации лекарств для оценки их влияния на метаболизм раковых клеток и рост опухоли25. Таким образом, доклиническое исследование заключалось в дальнейшей оценке влияния METABLOC в сочетании с новыми лекарственными средствами (Метформин и Диклофенак) на рост трансплантированной карциномы легких Льюиса LL/2 у мышей. Выбор этих двух препаратов основан на их положительном влиянии на замедление роста опухоли. Метформин — это старое лекарство, обычно используемое при диабете II типа [Исследовательская группа Программы по профилактике диабета]. Новые исследования показывают положительный эффект от использования Метформина в терапии рака26,27,28. Поскольку Метформин используется в качестве гипогликемического лекарственного средства при диабете II типа, он замедляет секрецию инсулина и пролиферацию клеток, разобщая митохондриальное дыхание и производство АТФ (фосфорилированием) на протяжении всей цепочки транспортировки электронов в митохондриях — ETC. Интересно, что ретроспективные эпидемиологические исследования показали, что у пациентов с диабетом при длительном лечении Метформином снижается риск развития рака26,29. Более того, другое доклиническое исследование показало антипролиферативное действие Метформина на ксенотрансплантат опухоли у мышей30. Диклофенак также является старым лекарственным средством, используемым в настоящее время в качестве противовоспалительного средства. Недавние исследования упоминали потенциальное использование Диклофенака в лечении рака31,32,33. Например, Gottfried et al. (2013) показали, что Диклофенак ослабляет эффект Варбурга, направляя транспорт глюкозы в раковые клетки и ингибируя лактатдегидрогеназу(ЛДГ)/(lactate dehydrogenase (LDH)) и монокарбоксилатный транспортер 1 (МСТ1). Это приводит к снижению поглощения глюкозы и секреции лактата.
В этой работе мы вводили ксенотрансплантат клеток карциномы легкого Lewis LL/2 в брюшную полость мышей и тестировали влияние различных комбинаций препаратов на эволюцию объема опухоли. Результаты показывают уменьшение объема опухоли LL/2 при введении МЕТАБЛОКА в сочетании с Диклофенаком и Метформином. Эффект METABLOC усиливается, когда Метформин используется в высоких дозах. Результаты сравниваются с результатом введения классического химиотерапевтического агента (Цисплатина) в качестве положительного контроля. Мы также создали кинетическую метаболическую модель роста опухоли, чтобы охарактеризовать влияние метаболической терапии на метаболизм опухоли. Модель была не только способна моделировать рост опухоли в соответствии с экспериментальными данными, но также позволяла моделировать ингибирование роста после применения метаболической терапии. Такой подход к кинетическому моделированию роста опухоли открывает возможности для выявления новых метаболических мишеней.
Результаты
Высокие дозы Метформина и Диклофенака вызывают небольшую регрессию опухоли
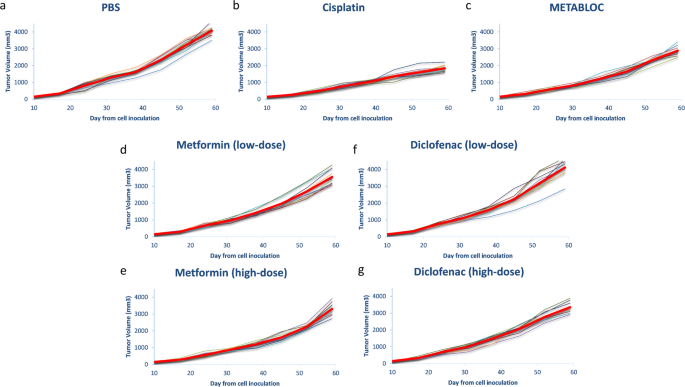
Сначала мы проанализировали эффект воздействия постояно низких и высоких доз Метформина и Диклофенака на группы мышей C57BL/6 (n = 10), несущих ксенотрансплантат опухоли легких Льюиса LL/2. В качестве контроля мы также создали группы для постоянного введения инъекциями (chronic injection) фосфатно-солевого буфера (PBS), Цисплатина (химиотерапевтический препарат) и METABLOC (гидроксицитрат кальция + липоевая кислота). Результаты представлены на рис. 1. У мышей, получавшие PBS в качестве отрицательного контроля, опухоли достигли объема 4000 мм3, тогда как группа, получавшая Цисплатин (положительный контроль), имела половину объема опухоли на 59 день (рис.1a,b). Мы также применили постоянную дозу METABLOC, уже использованную в наших предыдущих исследованиях. Эта комбинация цитрата кальция (HCA) и липоевой кислоты (ALA) действительно снижает рост опухоли, как сообщалось в наших предыдущих работах (Fig. 1c). Высокие дозы Метформина и Диклофенака слегка задерживают рост опухоли с 10 по 59 день после инокуляции клеток (рис. 1e,g). Низкие дозы Метформина также задерживают рост опухоли, но не низкие дозы Диклофенака (Fig. 11d,f). Метформин демонстрирует эффект доза-ответ на объем опухоли (3500 мм3 для низкой дозы и 3300 мм3 для высокой дозы). Это не тот случай, когда группа, получавшая Диклофенак, где высокая доза Диклофенака немного уменьшает объем опухоли (среднее значение = 3300 мм3), но группа с низкой дозой аналогична PBS на 59 день (рис. 1). Эксперименты были остановлены на 59 день, так как группа PBS достигает летального объема опухоли. Затем другую группу кормили METABLOC, давали Метформин или Диклофенак.
Эволюция опухоли ксенотрансплантата у мышей при метаболической терапии. Лечение начинали на двенадцатый день после инокуляции мышей. Тонкие кривые представляют объемы опухолей для каждой отдельной мыши. Красные жирные кривые — это средние значения всех тонких кривых. (а) Фосфатно-солевой буфер (PBS) используется в качестве контроля. (b) Химиотерапевтическое средство Цисплатин замедляет рост опухоли. (c) Рост опухоли слегка снижается при терапии METABLOC. (d – g) Метформин в низких и высоких дозах и Диклофенак не оказывают существенного влияния на развитие опухоли.
METABLOC and high-dose Metformin combination slows and inhibits tumor growth
Комббинация МЕТАБЛОК и Метформина замедляет и ингибирует рост опухоли.
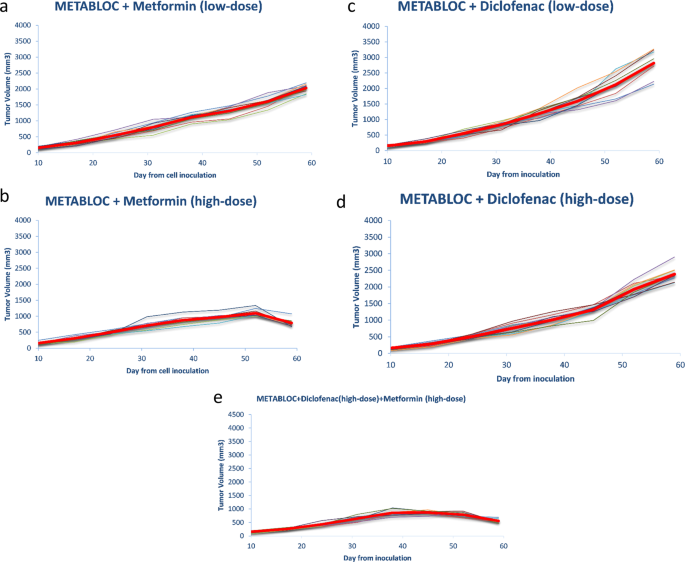
Комбинация METABLOC с высокими дозами Метформина и Диклофенака значительно задерживает прогрессирование карциномы LL/2 у мышей по сравнению с лечением с применением фосфатно-солевого буфера (PBS) или METABLOC (Fig.2b,c). METABLOC в сочетании с низкими дозами Метформина также оказывает положительный эффект, тогда как его комбинация с низкими дозами Диклофенака оказывает слабое действие (Fig.2d). Эти кривые графиков показывают, что только в группе, получавшей METABLOC и в высокой дозе Метформин, наблюдается регресс в объеме опухоли (Fig.2b). Средний объем опухоли значительно уменьшился с 45 дня до 59 дня на комбинации METABLOC + Метформин (высокая доза) (p <0,005). Опухоль имела лучшую реакцию на нашу комбинацию по сравнению с лечением Цисплатином (р <0,001). Высокие дозы Метформина явно усиливают нашу предыдущую комбинацию METABLOC (гидроксицитрат + липоевая кислота).
Эволюция опухоли при комбинациях метаболических терапий. Тонкие кривые представляют объемы опухолей для каждой отдельной мыши. Красные жирные кривые — это средние значения всех тонких кривых. (а) METABLOC + низкие дозы Метформина замедляет рост опухоли. (b) METABLOC + высокая доза Метформина значительно снижает развитие опухоли и ингибирует рост опухоли на 50-й день после инокуляции клеток. (c,d) METABLOC + низкодозированный и высокодозированный Диклоненак не оказывает существенного влияния на ингибирование роста опухоли. (e) METABLOC + высокие дозы Метформина и Диклофенака значительно подавляют рост опухоли и обращают вспять опухолевую кривую.
Высокая доза Диклофенака усиливает ингибирующий эффект Метформина на рост опухоли.
Мы пошли дальше в нашем исследовании и лечили группу мышей (n = 10) полной комбинацией METABLOC + Метформин (низкая и высокая дозы) + Диклофенак. Добавление высокой дозы Диклофенака к METABLOC + высокая доза Метформина улучшила реакцию опухоли на лечение (рис. 2e). Объем опухоли начинает регрессировать на 45 день в группе, получавшей METABLOCS (METABLOC + Метформин (высокая доза) + Диклофенак (высокая доза)), тогда как эта регрессия наблюдается на 52 день для комбинации METABLOC + Метформин (высокая доза) (Рис. 2b) , Комбинация с низкими дозами метформина менее выражена. METABLOCS значительно уменьшает рост опухоли на 59-й день по сравнению с METABLOC + Метформин с высокой дозой (p <0,001) (Fig. 2b). По сравнению с лечением Цисплатином METABLOC обладает меньшим эффектом, но чувствительность опухолевых клеток увеличивается, когда последний комбинируется с Метформином, а затем с Метформином + Диклофенак. Комбинации этих старых и недорогих препаратов в два раза эффективнее, чем классический химиотерапевтический агент. Наш новый вывод заключается в том, что комбинация METABLOC (гидроксицитрат + липоевая кислота) и высоких доз Метформина сильно ингибирует рост ксенотрансплантата опухоли, инокулированного группе мышей (n = 10).
In silico (исследование выполнено на компьютере или с помощью компьютерного моделирования Г.Л.) метаболическая терапия симулирует ингибирование роста раковой опухоли.
Кинетическая метаболическая модель (см. Метаболическую сеть на рис.3 и систему дифференциальных уравнений в методах) была создана на основе предыдущих моделей, описывающих рост клеток яичника китайского хомячка (СНО) в различных средах для получения моноклональных антител 34, Здесь наша модель впервые используется для моделирования роста ксенотрансплантата опухоли, имплантированной группе мышей. Затем модель использовалась для моделирования влияния метаболической терапии in silico — METABLOC — Metformin — Diclofenac на рост опухоли. Эта модель полезна не только для моделирования экспериментально полученного роста опухоли, но и позволяет нам характеризовать метаболические фенотипы опухоли, развивающейся у мышей со временем.
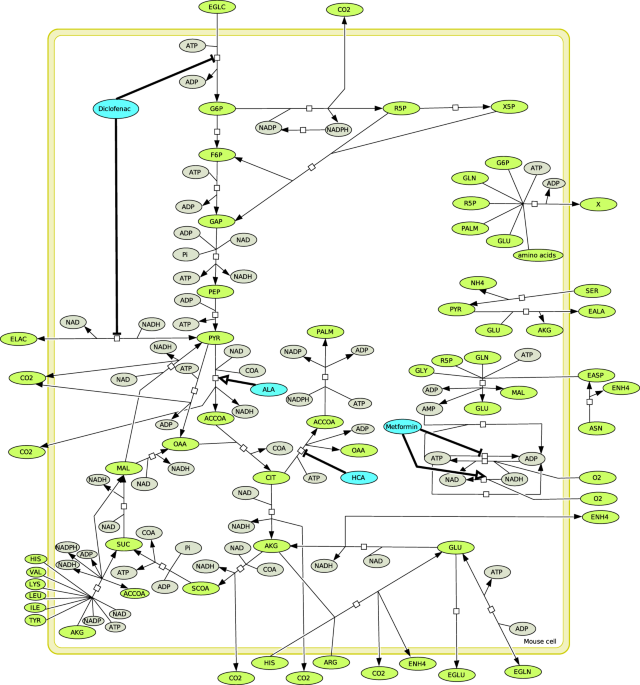
Метаболическая сеть. Основной метаболизм раковых клеток включает гликолиз, пентозофосфатный путь, цикл лимонной кислоты, липогенез и метаболизм аминокислот. Синтез биомассы описывается как инкорпорирование аминокислот, промежуточных метаболитов и пальмитиновой кислоты. Метаболическая терапия включает Диклофенак в качестве ингибитора гексокиназы и лактатдегидрогеназы; альфа-липоевую кислоту (ALK) (alpha-Lipoic acid (ALA)) в качестве активатора пируватдегидрогеназы; Гидроксицитрат (ГКА) (Hydroxycitrate (HCA)) в качестве ингибитора АТФ(ATP citrate lyase inhibitor)-цитрат-лиазы; Метформин как ингибитор АТФ-синтазы(ATP synthase) и активатор утечки НАД (NAD).
Обозначения:
ACCOA: ацетил-коэнзим A(Acetyl-CoenzymeA),
ACCOA: Ацетил-Кофермент A(Acetyl-CoenzymeA),
ACL: АТФ-цитратлиаза(ATP-citrate lyase),
ADP: Аденозиндифосфат (Adenosine diphosphate)
AK: Аденилаткиназа (Adenylate kinase),
AKG: α-кетоглутарат,
ALA: Внеклеточный Аланин,
AMP: Аденозин Монофосфат: Аденозин Монофосфат: Аденозин Монофен Аргинин,
ASN: Аспарагиназа,
ASP: внеклеточный аспартат,
ATP: аденозинтрифосфат,
CIT: цитрат, CO2: диоксид карбона,
DICLO: внеклеточный Диклофенак,
EGLC: внеклеточная глюкоза (Extracellular glucose),
EGLN: внеклеточный глютамин,
EGLU: внеклеточный глутамат,
F6P — Фосфат,
FADH2: флавин-аденин-динуклеотид,
FUM: фумарат, G6P: глюкозо-6-фосфат,
GAP: глицеральдегид-3-фосфат, концентрация,
GlnT: Глутамин-синтетаза,
GLU: глутамат,
GLY: Внеклеточный Глицин,
H2O: Диоксид Водорода :Внеклеточный Гидроксицитрат,
HIS: Внеклеточный Гистидин,
HISARGTA: Трансаминирование Гистидина / Аргинина,
ILE: Внеклеточный Изолейцин,
LA: Внеклеточная Липоевая кислота,
LAC: Внеклеточный Лактат,
LEU: внеклеточный лейцин,
LYS: внеклеточный лизин,
MAL: малат,
ME: малеиновый фермент,
Метформин: внеклеточной метформин,
NAD: Никотинамид-аденин-динуклеотид (окисленный) (Nicotinamide adenine dinucleotide (Oxidized)),
NADH: Никотинамид-аденин-динуклеотид (восстановленный) Nicotinamide adenine dinucleotide (reduced),
NADP: никтинамид аденин динуклеотид фосфат (nictoniamide adenine dinucleottide phosphate),
NADPH: никтинамид аденин динуклеотид фосфат (восстановленный) (nictoniamide adenine dinucleotide phosphate (reduced)),
NH4: внеклеточной аммиак (Extracellular ammonia),
OXA: Оксалоацетат(Oxaloacetate),
PALM: Пальмитат(Palmitate),
PEP: Фосфоенолпируват(Phosphoenolpyruvate),
Pi: Неорганический фосфат(inorganic phosphate),
PK: Пируваткиназа(Pyruvate kinase),
PPRibP: Синтез нуклеотидов(Nucleotide synthesis),
PYR: Пируват(Pyruvate),
R5P: Рибулозо-5-фосфат(Ribulose-5-phosphate),
SER: Внеклеточный серин (Extracellular serine),
SUC:Сукцинат, (succinate,SUCCOA)
Сукцинил-кофермент A (Succinyl coenzyme A),
THR: Внеклеточный треонин, (Extracellular threonine ),
TYR : Внеклеточный Тирозин, (Extracellular tyrosine),
VAL: Внеклеточный валин. (Extracellular valine).
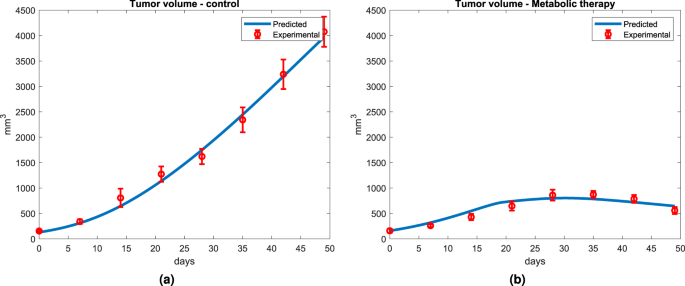
Модель адекватно имитирует рост ксенотрансплантата опухоли у мышей для наиболее эффективной стратегии лечения (рис.4a). Прогнозируемый объем опухоли находится в пределах стандартных отклонений экспериментального объема опухоли. Модель предсказывает эволюцию объема опухоли от 154 мм3 до 3900 мм3 в соответствии с экспериментальными данными (от 154 ± 16 до 4076 ± 297 мм3). Важно отметить, что модельные прогнозы основаны только на общем объеме опухолевых клеток и кровеносной сети капилляров. Таким образом, результаты подтверждают способность модели описывать рост опухоли. Для модели, интегрирующей метаболическую терапию, терапевтические молекулы поставляются во входном потоке крови (F), питающем объем крови капилляров (то есть микроокружение опухолевых клеток). Известно, что эти молекулы специфически нацелены на определенные ферментативные пути; с известными эффектами на клеточный метаболизм, которые подробно описаны в модели. Модельное моделирование описывает ингибирование роста опухоли метаболической терапией (METABLOC + Metformin + Diclofenac). Рис.4b. Как экспериментальные, так и прогнозируемые данные эволюции опухоли показывают уменьшенную фазу роста от t0 (10 дней после инокуляции опухоли) и достигают плато на 35-й день. Имитация ситуации с использованием модели предсказывает плато роста на уровне около 873 мм3, как и для экспериментальных данных (873 ± 70 мм3). ). Однако модель не предсказывает уменьшение объема опухоли. Вероятно, это связано с возникновением апоптоза в опухоли, феномен, который не описан в модели.
Прогнозы роста опухоли в контрольной и in silico метаболической терапии. (а) Кинетическая модель метаболизма опухоли предсказывает объем опухоли в соответствии с экспериментальными данными. (b) При метаболической терапии (METABLOC в сочетании с Диклофенаком и высокой дозой Метформина) модель предсказывает ингибирование опухоли и регрессию ее объема, как и было определено экспериментально.
Метаболическая модель предсказывает обратный эффект Варбурга при метаболической терапии
Метаболическая модель предсказывает обратный эффект Варбурга на метаболическую терапию.
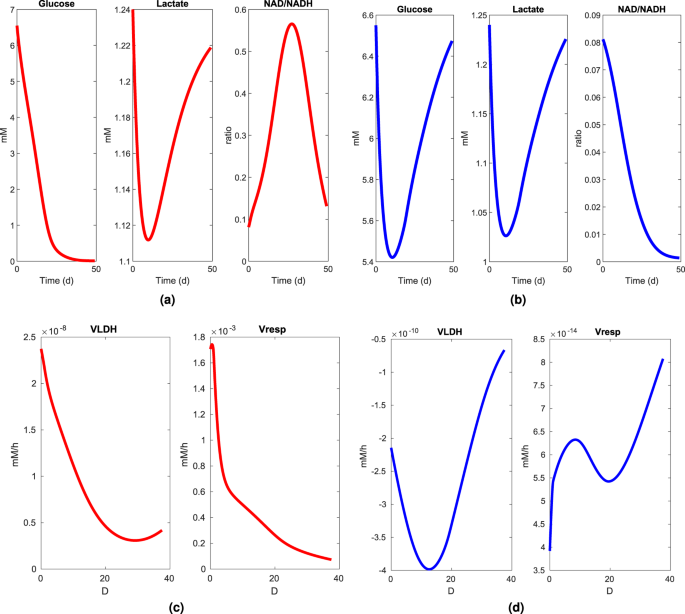
В недавней работе35 мы сообщили о концентрациях ключевых метаболитов, участвующих в управлении энергией во всем центральном (базовом) углеродном обмене. Концентрации аденозинтрифосфата (АТФ), никотинамидадениндинуклеотида (NAD) и никотинамидадениндинуклеотидфосфата (NADP) были измерены в нормальных и раковых клетках, выделенных из свежих тканей толстой кишки человека. Наши результаты показали высокое окислительно-восстановительное отношение NAD+-относительно-NADH (иначе NAD+/NADH) и NADP+-относительно-NADPH (иначе NAD+/NADH) в популяциях раковых клеток по сравнению с нормальными пролиферирующими клетками. Интересно, что наша модель также предсказывает высокопроизводительный аэробный гликолиз, широко известный как эффект Варбурга, наблюдаемый в раковых клетках (рис. 5 (a,c)). Потребление глюкозы опухолевыми клетками является линейным до достижения уровня ограничения в конце 25-го дня и полностью потребляется через 59 дней после инкубации. Этот ускоренный гликолиз приводит к массивному выделению и накоплению лактата в кровотоке. Отношение NAD+/NADH является катаболическим маркером этого аэробного гликолиза, предложенного Варбургом в его оригинальной статье16. Следовательно, важное соотношение NAD+/NADH позволяет поддерживать гликолитический потенциал раковых клеток. Сочетание METABLOC и высоких доз метформина и диклоненака значительно снижает потребление глюкозы опухолевыми клетками. Таким образом, это явление приводит к снижению секреции и накопления лактата (Fig. 5 (b,d)). Редокс-отношение NAD+/NADH является низким и уменьшается при метаболической терапии. Эти наблюдения являются одновременно признаками уменьшенного гликолитического потока или обратного эффекта Варбурга.
Смоделированные метаболиты крови (глюкоза и лактат) и смоделированное окислительно-восстановительное отношение (NAD+/NADH) в опухоли (а) и опухоли, получавших метаболические препараты (b). Смоделированные пути лактатдегидрогеназы (VLDH) и дыхания (Vresp) в опухоли (c) и опухоли, обработанной метаболическими препаратами (d). (а) Молочная кислота сначала удаляется кровотоком, а затем накапливается с ростом опухоли. Соотношение NAD+/NADH уменьшается при истощении глюкозы. (b) При метаболической терапии замедляется поглощение глюкозы, а также секреция молочной кислоты. Соотношение NAD+/NADH уменьшается с ростом опухоли. (c) Высокое значение лактатдегидрогеназы (VLDH) и уменьшение пути дыхания являются маркерами эффекта Варбурга в опухоли. (d) Отрицательный значение потока лактатдегидрогеназы (VLDH), который соответствует поглощению лактата и увеличению потока дыхания, транслирует обратный эффект Варбурга.
Заключение
Метаболическая терапия была использована для изучения роста ксенографа опухоли у мышей. Мы экспериментально показали, что комбинация METABLOC, высоких доз Метформина и Диклофенака ингибирует рост опухоли. Мы предложили динамическую метаболическую модель опухоли, которая имитирует влияние метаболической терапии на развитие опухоли и метаболизм опухолевых клеток. Эта модель также предсказывает регрессию опухоли, более медленный гликолитический поток (ниже скорость, с которой молекулы проходят через гликолитический путь) и меньшее количество секреции молочной кислоты при метаболических воздействиях. Внутриклеточное окислительно-восстановительное отношение NAD+/NADH является низким и уменьшается, как следствие замедления гликолитического потока. Действительно, окислительное фосфорилирование может быть возвращено назад с пути ферментации, способствуя митохондриальному дыханию и обратному эффекту Варбурга. Наша модель поддерживает наши экспериментальные результаты и может также использоваться для тестирования новой комбинации метаболических методов лечения. Эти результаты открывают путь для новых стратегий в метаболической терапии и разработке метаболических препаратов in silico.
Методы
Клеточная Культура
Клеточную линию LLC/1 ATCC® CRL-1642 (LGC Standards, Molsheim-France), культивируемая в среде DMEM Glutamax I (Invitrogen-Gibco) с 10% FBS (Eurobio) и 1/10000 МЕ пенициллина/стрептомицина ( Sigma Aldrich (P4333) вводили инъециями в брюшную полость мышей из расчета 5 миллионов клеток на мышь за 150 уколов и в пределах 12 дней после инкубации, когда опухоли достигали 130 мм3, мышей рандомизировали и начинали лечение.
Метаболическое воздействие
Липоевую кислоту (Sigma Aldrich T1395), гидроксицитрат кальция (IWDO) и Цисплатин (Sigma Aldrich 479306) растворяли в PBS и вводили внутрибрюшинно (i.p.) два раза в день (2X / D) для липоевой кислоты и гидроксицитрата кальция, 1X/2D для Цисплатина в дозе 10 мг / кг, 250 мг / кг и 1 мг/кг соответственно. Капли этанола добавляли для полного растворения липоевой кислоты в растворе фосфатно-солевого буфера PBS. Диклофенак натрия (Sigma-Aldrich 93484) в дозе 3 мг / кг и 30 мг / кг с поправкой на 25 μL/мл (LOW) и 250 μл/мл (HIGH) питьевой воды вводили перорально (Per Os). Мышь пьет около 3 мл воды в день. Метформин (Sigma-Aldrich 1396309) в дозах 2,5 мг/кг, 12,5 мг/кг и 25 мг/кг, скорректированных на 20 μ/мл (LOW), 100 μл/мл (MEDIUM) и 200 μл/мл (HIGH) питьевой воды также вводили перорально.
Обращение с животными
Мышей рассортировали по весу на группы по 10 животных на группу. Сорок восемь групп инбредных самцов мышей C57BL/6 в возрасте 6–8 недель (средний вес: 21,15 ± 1,11 г) были получены из Института Пастера, Иран. Их поместили по пять особей в клетку с доступом к автоклавированному корму для мышей и воде ad libitum (по желанию без ограничений). Их содержали в помещении при контролируемой температуре (22° C), влажности (55%) и освещении (свет — с 7:00 до 7:00). Все животные получали уход в соответствии с Руководством по уходу и использованию лабораторных животных [Публикация DHEW № (NIH) 85–23, 1985 г. со всеми последующими обновлениями, Отчеты Управления науки и здравоохранения, DRR/NIH, Bethesda, MD 20205]. Протоколы экспериментов были одобрены компанией Nosco Pharmaceuticals.
Метаболическая система взаимодействий
Метаболическая сеть, представленная здесь и показанная на рис. 3, была модифицирована на основе предыдущих моделей клеток яичника китайского хомячка (Chinese Hamster Ovary cells — СНО) и мышечных супрессорных клеток (MD-SC), полученных из миелоидных клеток 34,36,37,38,39. Включает 35 ферментативных реакций, описывающих судьбу 52 метаболитов. Мы выделили две группы: внешние метаболиты (то есть микроокружение опухолевых клеток крови) и внутриклеточные метаболиты клеток с клеткой в качестве уникального компартмента. Сеть объединяет пути центрального углеродного метаболизма (central carbon metabolism CCM), такие как гликолиз, пентозофосфатный путь, цикл трикарбоновых кислот, липогенез, окислительное фосфорилирование и пути аминокислотного метаболизма. В этом центрального углеродного метаболизме ССМ глюкоза и аминокислоты являются основными источниками углерода и азота для пролиферации клеток и синтеза биомассы. Для получения дополнительной информации см.34.
Minimal cut sets of the metabolic networks
Минимальные цели воздействия в метаболической сети
Концепция минимального набора целей воздействия (Minimal cut sets) была введена для определения минимального набора реакций, удаление которых полностью блокирует мишень воздействия 40. В нашей метаболической сети есть 1058 минимальных целей воздействия, которые предотвращают рост опухоли (X). Они были рассчитаны с CellNetAnalyzer41,42, и мы выбрали самый короткий. Двадцать из них имеют размер меньше двух, и только 6 имеют размер единица: VHK, VG6PDH, VCS, VACL, VPALM, Vgrowth. Поскольку наша терапия не является генетической модификацией, ингибирование одной из целей воздействия не будет полностью предотвращать рост опухоли. Этот структурный анализ показывает, что Диклофенак, который ингибирует гексокиназу (VHK), и Гидроксицитрат, который ингибирует АТФ-цитрат лиазу (VACL), должны оказывать негативное влияние на рост опухоли.
Динамическое моделирование объема опухоли
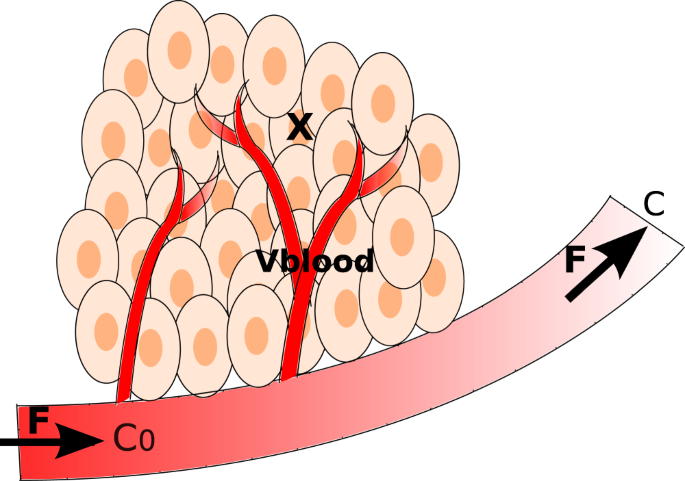
Объем опухоли включает раковые клетки и сеть капилляров (рис. 6). Модель была создана на основе баланса массы по метаболитам и концентрации опухолевых клеток. Опухолевые клетки непрерывно перфузируют из сети капилляров общего объема Vb, которая рассматривается как идеально перемешанный реактор с мешалкой (CSTR). Таким образом, состав крови в объеме опухоли считался однородным. В перфузионной системе клетки удерживаются в сосуде.
Опухоль непрерывно питается сетью капилляров с общей скоростью кровотока (F) композиции C на входе в кровоток опухоли. Для упрощения пренебрегли изменением кровотока с ростом опухоли. Здесь C и C — векторы концентраций опухолевой крови и концентраций в крови в метаболитах на входе опухоли соответственно (в мМ), а m — вектор концентраций внутриклеточных метаболитов опухолевых клеток (в мМ). Sc и Sm представляют собой стехиометрические матрицы реакций с участием внеклеточных и внутриклеточных метаболитов соответственно. Термин r представляет собой вектор удельных скоростей (в mM/h клетках и mmol/1(h−1) cells/h в капилярах) каждой реакции в метаболической сети, тогда как µ и μblood представляют собой удельные темпы роста или увеличения объема клеток и капилляров (h−1) соответственно. Х это общий объем опухолевых клеток (в 106 клеток/мл), а εm — доля внутриклеточных метаболитов, которые интегрированы в вещество клеток. Динамическая система написана следующим образом и объясняется в дополнительных материалах:
Parameter estimation
Приблизительная оценка параметров
Значение параметра, где оно впервые взято из предыдущих работ о клетках СНО 34,36, когда оно не доступно для рака или клеток человека в литературе или банках данных. Затем мы использовали функцию нелинейной оптимизации fmincon (MatWorks®) для оптимизации чувствительных параметров, таких как Fin, Fout, и удельная скорость роста опухолевых клеток (μ). Оптимизация значения параметров основывалась на следующей целевой функции:
где Yexpn,t представляет собой nth экспериментальные данные в tth время эксперимента, Yn,t(p) — смоделированный выходной сигнал с «p» вектором трех чувствительных параметров и «σ» — стандартным отклонением экспериментальных измерений.
Дополнительная информация:
Publisher’s note: Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Ссылки:
- 1.
Seyfried, T. N. & Shelton, L. M. Cancer as a metabolic disease. Nutr. & Metab. 7, 7, https://doi.org/10.1186/1743-7075-7-7 (2010).
- 2.
Gatenby, R. A. Is the Genetic Paradigm of Cancer Complete? Radiology 284, 1–3, https://doi.org/10.1148/radiol.2017171004 (2017).
- 3.
Oppermann, H., Levinson, A. D., Varmus, H. E., Levintow, L. & Bishop, J. M. Uninfected vertebrate cells contain a protein that is closely related to the product of the avian sarcoma virus transforming gene (src). Proc. Natl. Acad. Sci. United States Am. 76, 1804–1808 (1979).
- 4.
Lander, E. S. et al. Initial sequencing and analysis of the human genome. Nature 409, 860–921, https://doi.org/10.1038/35057062 (2001).
- 5.
Hanahan, D. & Weinberg, R. A. The hallmarks of cancer. Cell 100, 57–70 (2000).
- 6.
Hanahan, D. & Weinberg, R. A. Hallmarks of cancer: the next generation. Cell 144, 646–674, https://doi.org/10.1016/j.cell.2011.02.013 (2011).
- 7.
Balkwill, F. & Mantovani, A. Inflammation and cancer: back to Virchow? Lancet (London, England) 357, 539–545, https://doi.org/10.1016/S0140-6736 (2001).
- 8.
Abolhassani, M. et al. Hyperosmolarity causes inflammation through the methylation of protein phosphatase 2a. Inflamm. Res. Off. J. Eur. Histamine Res. Soc. et al. 57, 419–429, https://doi.org/10.1007/s00011-007-7213-0 (2008).
- 9.
Abolhassani, M., Guais, A., Chaumet-Riffaud, P., Sasco, A. J. & Schwartz, L. Carbon dioxide inhalation causes pulmonary inflammation. Am. J. Physiol. Lung Cell. Mol. Physiol. 296, L657–665, https://doi.org/10.1152/ajplung.90460.2008 (2009).
- 10.
Schwartz, L. et al. Hyperosmotic stress contributes to mouse colonic inflammation through the methylation of protein phosphatase 2a. Am. J. Physiol. Gastrointest. Liver Physiol. 295, G934–941, https://doi.org/10.1152/ajpgi.90296.2008 (2008).
- 11.
Schwartz, L., Guais, A., Pooya, M. & Abolhassani, M. Is inflammation a consequence of extracellular hyperosmolarity? J. Inflamm. (London, England) 6, 21, https://doi.org/10.1186/1476-9255-6-21 (2009).
- 12.
Israël, M. & Schwartz, L. The metabolic advantage of tumor cells. Mol. Cancer 10, 70, https://doi.org/10.1186/1476-4598-10-70 (2011).
- 13.
Israël, M. A possible primary cause of cancer: deficient cellular interactions in endocrine pancreas. Mol. Cancer 11, 63, https://doi.org/10.1186/1476-4598-11-63 (2012).
- 14.
Israel, M. Comment on cancer metabolism and on the role of the endocrine pancreas. J. Clin. Medicine Res. 6, 490–491, https://doi.org/10.14740/jocmr1912w (2014).
- 15.
Warburg, O., Wind, F. & Negelein, E. The Metabolism Of Tumors In The Body. The J. Gen. Physiol. 8, 519–530 (1927).
- 16.
Warburg, O. On the origin of cancer cells. Sci. (New York, N.Y.) 123, 309–314 (1956).
- 17.
Gatenby, R. A. & Frieden, B. R. Information dynamics in carcinogenesis and tumor growth. Mutat. Res. 568, 259–273, https://doi.org/10.1016/j.mrfmmm.2004.04.018 (2004).
- 18.
Deberardinis, R. J., Sayed, N., Ditsworth, D. & Thompson, C. B. Brick by brick: metabolism and tumor cell growth. Curr. Opin. Genet. & Dev. 18, 54–61, https://doi.org/10.1016/j.gde.2008.02.003 (2008).
- 19.
Kroemer, G. & Pouyssegur, J. Tumor cell metabolism: cancer’s Achilles’ heel. Cancer Cell 13, 472–482, https://doi.org/10.1016/j.ccr.2008.05.005 (2008).
- 20.
da Veiga Moreira, J. et al. Cell cycle progression is regulated by intertwined redox oscillators. Theor. Biol. Med. Model. 12, 10, https://doi.org/10.1186/s12976-015-0005-2 (2015).
- 21.
Schwartz, L. et al. A combination of alpha lipoic acid and calcium hydroxycitrate is efficient against mouse cancer models: preliminary results. Oncol. Reports 23, 1407–1416 (2010).
- 22.
Hatzivassiliou, G. et al. ATP citrate lyase inhibition can suppress tumor cell growth. Cancer Cell 8, 311–321, https://doi.org/10.1016/j.ccr.2005.09.008 (2005).
- 23.
Bonnet, S. et al. An abnormal mitochondrial-hypoxia inducible factor-1alpha-Kv channel pathway disrupts oxygen sensing and triggers pulmonary arterial hypertension in fawn hooded rats: similarities to human pulmonary arterial hypertension. Circulation 113, 2630–2641, https://doi.org/10.1161/CIRCULATIONAHA.105.609008 (2006).
- 24.
Guais, A. et al. Adding a combination of hydroxycitrate and lipoic acid (METABLOCTM) to chemotherapy improves effectiveness against tumor development: experimental results and case report. Investig. New Drugs 30, 200–211, https://doi.org/10.1007/s10637-010-9552-x (2012).
- 25.
Abolhassani, M. et al. Screening of well-established drugs targeting cancer metabolism: reproducibility of the efficacy of a highly effective drug combination in mice. Investig. New Drugs 30, 1331–1342, https://doi.org/10.1007/s10637-011-9692-7 (2012).
- 26.
Evans, J. M. M., Donnelly, L. A., Emslie-Smith, A. M., Alessi, D. R. & Morris, A. D. Metformin and reduced risk of cancer in diabetic patients. BMJ 330, 1304–1305, https://doi.org/10.1136/bmj.38415.708634.F7 (2005).
- 27.
Sahra, I. B., Marchand-Brustel, Y. L., Tanti, J.-F. & Bost, F. Metformin in Cancer Therapy: A New Perspective for an Old Antidiabetic Drug? Mol. Cancer Ther. 9, 1092–1099, https://doi.org/10.1158/1535-7163.MCT-09-1186 (2010).
- 28.
Loubiere, C., Dirat, B., Tanti, J. & Bost, F. Metformine et cancer: passé, présent, avenir. Obesite 3, 205–213 (2014).
- 29.
Libby, G. et al. New Users of Metformin Are at Low Risk of Incident Cancer A cohort study among people with type 2 diabetes. Diabetes Care 32, 1620–1625, https://doi.org/10.2337/dc08-2175 (2009).
- 30.
Krisztina, K., Aune, M., James, S.-S., Guido, E. & Enrique, R. Metformin Inhibits the Growth of Human Pancreatic Cancer Xenografts. Pancreas 42, 781–785, https://doi.org/10.1097/MPA.0b013e31827aec40 (2013).
- 31.
Gottfried, E. et al. New aspects of an old drug–diclofenac targets MYC and glucose metabolism in tumor cells. PloS One 8, e66987, https://doi.org/10.1371/journal.pone.0066987 (2013).
- 32.
Mayorek, N., Naftali-Shani, N. & Grunewald, M. Diclofenac inhibits tumor growth in a murine model of pancreatic cancer by modulation of VEGF levels and arginase activity. PloS One 5, e12715, https://doi.org/10.1371/journal.pone.0012715 (2010).
- 33.
Al-Nimer, M. S., Hameed, H. G. & Mahmood, M. M. Antiproliferative effects of aspirin and diclofenac against the growth of cancer and fibroblast cells: In vitro comparative study. Saudi. Pharm. J. 23, 483–486, https://doi.org/10.1016/j.jsps.2015.01.002 (2015).
- 34.
Robitaille, J., Chen, J. & Jolicoeur, M. A Single Dynamic Metabolic Model Can Describe mAb Producing CHO Cell Batch and Fed-Batch Cultures on Different Culture Media. PloS One 10, e0136815, https://doi.org/10.1371/journal.pone.0136815 (2015).
- 35.
da Veiga Moreira, J. et al. The Redox Status of Cancer Cells Supports Mechanisms behind the Warburg Effect. Metabolites 6, https://doi.org/10.3390/metabo6040033 (2016).
- 36.
Ghorbaniaghdam, A., Henry, O. & Jolicoeur, M. A kinetic-metabolic model based on cell energetic state: study of CHO cell behavior under Na-butyrate stimulation. Bioprocess Biosyst. Eng. 36, 469–487, https://doi.org/10.1007/s00449-012-0804-3 (2013).
- 37.
Ghorbaniaghdam, A., Chen, J., Henry, O. & Jolicoeur, M. Analyzing clonal variation of monoclonal antibody-producing CHO cell lines using an in silico metabolomic platform. PloS One 9, e90832, https://doi.org/10.1371/journal.pone.0090832 (2014).
- 38.
Ghorbaniaghdam, A., Henry, O. & Jolicoeur, M. An in-silico study of the regulation of CHO cells glycolysis. J. Theor. Biol. 357, 112–122, https://doi.org/10.1016/j.jtbi.2014.04.035 (2014).
- 39.
Goffaux, G., Hammami, I. & Jolicoeur, M. A Dynamic Metabolic Flux Analysis of Myeloid-Derived Suppressor Cells Confirms Immunosuppression-Related Metabolic Plasticity. Sci. Reports 7, 9850, https://doi.org/10.1038/s41598-017-10464-1 (2017).
- 40.
Klamt, S. & Gilles, E. Minimal cut sets in biochemical reaction networks. Bioinformatics 20, 226–234 (2004).
- 41.
Klamt, S., Saez-Rodriguez, J. & Gilles, E. Structural and functional analysis of cellular networks with cellnetanalyzer. BMC Syst. Biol. 1, 2, https://doi.org/10.1186/1752-0509-1-2 (2007).
- 42.
von Kamp, A., Thiele, S., Hädicke, O. & Klamt, S. Use of cellnetanalyzer in biotechnology and metabolic engineering. J. Biotechnol. 261, 221–228, https://doi.org/10.1016/j.jbiotec.2017.05.001 Bioinformatics Solutions for Big Data Analysis in Life Sciences presented by the German Network for Bioinformatics Infrastructure (2017).
![]()